
Ученые давно интересовались кристаллической решеткой алмаза. Благодаря своим характеристикам камень имеет особые свойства и ценность. Существуют аллотропные модификации, используемые в промышленности, электронике, медицине, космонавтике, авиации. В настоящее время индустрия создания искусственных алмазов развивается, но это очень дорого.

Строение кристалла и способ образования
Алмазный камень представляет собой кубическую аллотропную форму углерода, шестого элемента периодической таблицы. Формируется после сверхбыстрого охлаждения под высоким давлением. Его добывают в кимберлитовых трубках, вертикальных образованиях, возникающих при прохождении магмы через земную кору.
Фраза «кристаллическая решетка алмаза» относится к пространственному расположению и составу атомов углерода, которые определяют твердость минерала.
По сути, алмаз является модификацией углерода.

К какому типу относится кристаллическая решетка алмаза
Минерал имеет атомарную кристаллическую решетку, то есть атомы углерода расположены в узлах.
Особенности строения кристаллической решетки алмаза определяют его прочность, так как каждый атом расположен в центре тетраэдра (треугольной или трехгранной пирамиды) и связан ковалентными связями. Каждый атом прочно связан с четырьмя соседними атомами.
Минерал плохо проводит или практически не проводит электричество (диэлектрик). Это связано с тем, что атомы находятся на одинаковом расстоянии друг от друга и свободных электронов нет.
Для алмаза характерна кубическая сингония, то есть элементарная ячейка представлена в виде куба.
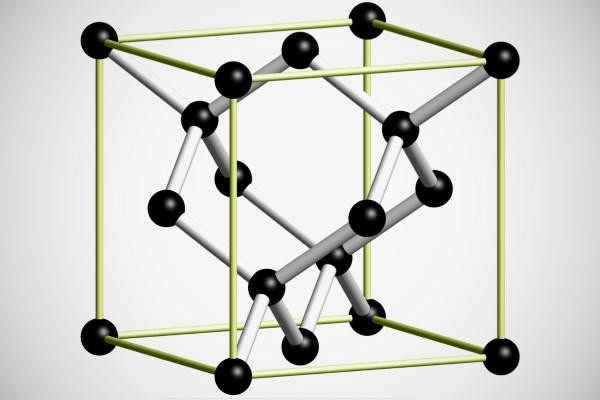
Структура кристаллической решетки алмаза:
- по одному атому углерода - на вершине куба;
- по одному атому на каждой грани;
- четыре атома находятся внутри куба.
Атомы, расположенные в центре граней, являются общими для двух ячеек. Атомы, расположенные в вершинах, являются общими для восьми ячеек. Между собой они связаны сильнейшим подвидом ковалентной связи — сигма-связью.
Всего химики различают 4 типа связей между атомами:
- ионный;
- металл;
- водород;
- ковалентный
Последний тип связи, образующий кристаллическую решетку алмаза, считается самым прочным.
Не все алмазы полностью состоят из углерода. Иногда в составе обнаруживаются посторонние примеси (кальций, алюминий, бор, магний, кремний, гранит, газы). Если на поверхности обнаружены загрязнения, их можно удалить в процессе резки. Будучи внутри камня, такие бриллианты не представляют ювелирной ценности и используются в промышленности.
Физические и химические свойства
Химическая формула минерала С. Кристалл хорошо проводит тепло, но не проводит (или слабо) электричество. Обладает хорошими преломляющими и отражающими свойствами.
Плавится при температуре выше 3700 градусов. Он горит в сочетании с кислородом при температуре более 721 градуса. Устойчив к кислотам и щелочам.
Физические свойства:
- Цвет: бесцветный, прозрачный. Возможны оттенки синего, желтого, голубого, розового, красного, коричневого, черного.
- Форма: кристалл с разным количеством граней.
- Блеск: сильный алмаз.
- Плотность: 3,5 г/см3.
- Твердость: абсолютная, 10 баллов. Но в то же время камень очень хрупкий.
- Вырез: Средний
- Электропроводность: слабая или отсутствует.
- Люминесценция в ультрафиолетовом свете.
- Под действием рентгеновских лучей прочность связи снижается.
Аллотропные модификации
Некоторые другие химические элементы имеют структуру, подобную алмазу, но немного другую молекулярную кристаллическую решетку. Разница в расположении атомов.
В алмазе атомы углерода расположены близко друг к другу. А у других элементов с большей атомной массой расстояние между атомами больше, что снижает их прочность.
Из известных аллотропных модификаций:
- Лонсдейлиты - недостаточно изучены, добыты из метеоритов или созданы искусственно, имеют гексагональную кристаллическую решетку.
- Графит: имеет схожую структуру, но отличается пи-связями и наличием свободных электронов (гексагональная кристаллическая решетка).
- Уголь используется в качестве сырья для производства тепла.
- Карабин - маленькие черные кристаллы в виде порошка, созданные искусственным путем.
- Фуллерены - кристаллическая решетка выглядит как шар, собранный из восьмиугольников, созданных искусственно.
- Углеродные нанотрубки используются в качестве каркаса для нанопродуктов.
Аллотропные модификации способны к трансформации: под воздействием температуры 1800 градусов превращаются в графит.
Способы применения вещества
Для производства ювелирных украшений используются высококачественно обработанные и ограненные камни, алмазы с идеальной кристаллической решеткой и составом (отсутствие примесей и изъянов). Это самая выгодная область применения минерала.
Неисправные камни идут на другие нужды:
- производство подшипников, сверл;
- использование в электронике и телекоммуникациях;
- производство механизмов из алмазной пыли;
- обрамляющие шлифовальные круги;
- создание оптических линз;
- использование в качестве абразивов;
- создание квантовых компьютеров;
- применение в ядерной энергетике;
- производство медицинских инструментов.
Получение искусственных минералов
В настоящее время разработаны способы получения алмаза из графита.
По методу HPHT формирование искусственного камня достигается выдержкой температуры 3000 градусов при давлении более 1000 Па и добавлением металлов. Это приводит к изменению ковалентных связей в кристаллической решетке и образованию пористых слизистых камней.
Получить небольшие, но геометрически совершенные и прозрачные драгоценные камни можно с помощью ударной волны (метод взрывного плавления).
Но считается, что лучший способ получить искусственные драгоценные камни — это вырастить их при температуре 1500 градусов. Но это дорогостоящий метод, как создание алмазов с помощью ультразвука. Поэтому камни принято получать из пара метана. Метод основан на нанесении графитовой пленки.
Технологии постоянно развиваются, и, возможно, в ближайшем будущем ученые научатся синтезировать искусственные алмазы с минимальными затратами.













